Что такое SPR-биосенсор, принцип работы и возможности использования.
Эффект поверхностного плазмонного резонанса (ППР, англ. SPR) играет важную роль в биологических исследованиях. Биосенсоры, принцип работы которых основан на этом эффекте, позволяют решать широкий круг задач: от качественного анализа до изучения кинетики и термодинамики взаимодействия лиганда с аналитом. Кроме того, в качестве аналита могут выступать не только низкомолекулярные соединения и макромолекулы, но и вирусы и даже бактерии. Как это работает?
Если на границе раздела двух фаз (например, между призмой и жидкостью) поместить тонкую плёнку из проводящего материала и направить излучение под бóльшим углом, чем требуется для отражения, небольшая часть этого излучения поглотится, а не отразится. Дело в том, что свободные электроны вблизи поверхности проводника непрерывно колеблются – эти колебания называют поверхностными плазмонами. Плазмоны характеризуются определёнными энергией и импульсом, и взаимодействие со светом с такими же параметрами приводит к их возбуждению. В результате излучение, падающее под определённым (резонансным) углом, поглощается, а возбуждение плазмонов порождает электромагнитную волну вблизи поверхности. В этом и состоит эффект поверхностного плазмонного резонанса.
Для практического применения важно, что возникающее электромагнитное поле крайне чувствительно к свойствам среды вплоть до ~300 нм от поверхности. Это поле влияет и на свойства плазмонов, поэтому любое взаимодействие в диапазоне ~300 нм сказывается на резонансном угле. Таким образом, если на поверхности проводника (обычно золота) закреплено соединение-лиганд, а в жидкой фазе содержится аналит, способный образовывать комплекс с лигандом, то это взаимодействие можно легко детектировать. Регистрация сигнала ведётся непрерывно, поскольку наиболее важная информация содержится в графиках временной зависимости сигнала – сенсограммы.
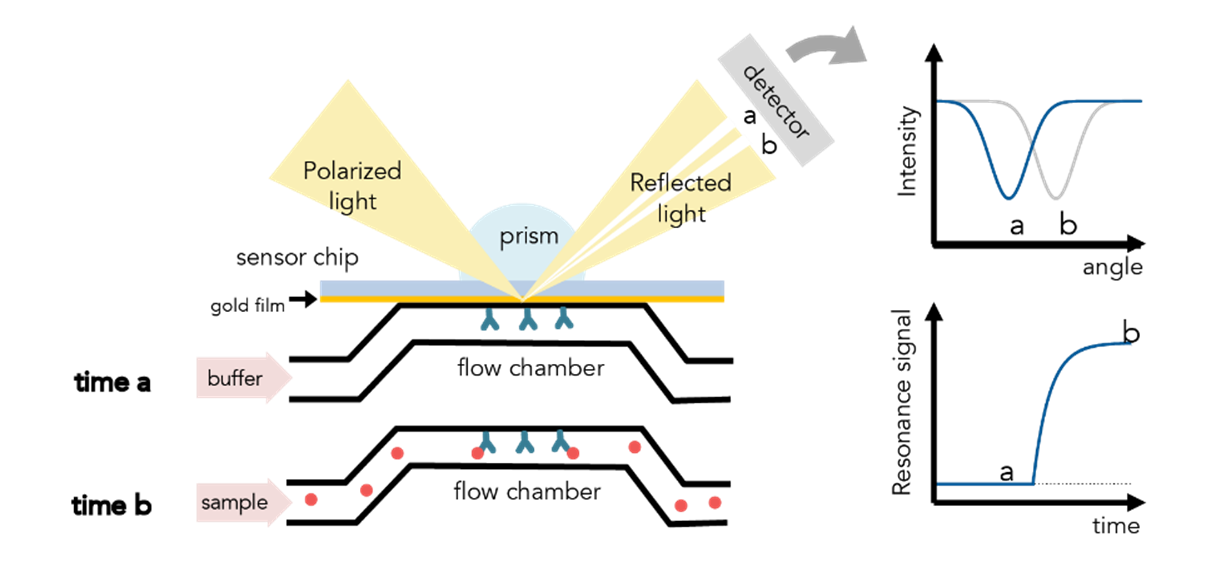
Рисунок 1. Схема регистрации сигнала с SPR-биосенсора
Биосенсоры на основе SPR позволяют анализировать межмолекулярные взаимодействия в самых разнообразных системах, таких как:
- антиген—антитело,
- белок-мишень и низкомолекулярное соединение (прототип лекарства),
- белок и нуклеиновая кислота,
- две разные нуклеиновые кислоты, и т.д.
Помимо этого, исследователю доступен анализ взаимодействий в мембранных системах, вирусах и бактериях. Помимо качественной оценки, с помощью SPR-биосенсора можно:
- определить термодинамические и кинетические параметры взаимодействия;
- осуществить первичный скрининг аналитов под конкретный лиганд;
- подобрать ингибитор под конкретную пару лиганд—аналит;
- провести количественный анализ аналита, построить калибровочные кривые, и т.д.
Кинетические и термодинамические параметры включают константы скоростей образования (ассоциации, kon) и распада комплексов (диссоциации, koff), равновесную константу диссоциации (KD), а также изменение свободной энергии Гиббса (ΔG). Прямое определение кинетических констант возможно благодаря проточной системе доставки вещества: сначала вводится раствор аналита, и на сенсограмме регистрируется образование комплексов, затем вводится буферный раствор, и на той же сенсограмме регистрируется их распад. Для определения KD, как правило, необходима серия экспериментов с различной концентрацией аналита, а для определения ΔG требуется зарегистрировать серию сенсограмм при разных температурах. Это несложные задачи, поскольку практически все процессы в современных SPR-биосенсорах автоматизированы. Кроме того, программное обеспечение позволяет автоматически обрабатывать сенсограммы и рассчитывать все необходимые параметры по различным моделям взаимодействий: для связывания одной или нескольких мишеней, конкурентное и бивалетное связывания, оценка steady-state и др.
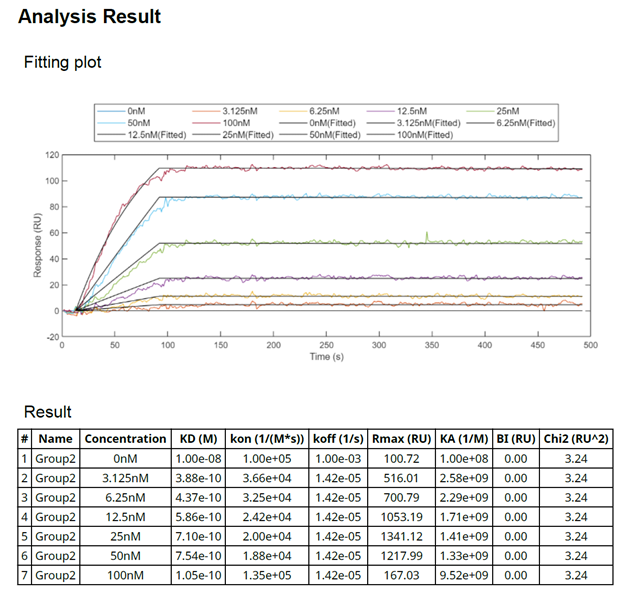
Рисунок 2. Качественные и количественные данные полученные с помощью SPR-биосенсора
Тем не менее, для корректной работы необходимо правильно подобрать сенсорный чип, поскольку для разных типов лигандов требуется различный тип поверхности. Например, немодифицированное золото применяется при самостоятельной разработке новой поверхности; золото, покрытое карбоксилированным декстраном, хорошо подходит для изучения межмолекулярных взаимодействий в белках и в системе белок—лекарство; гидрофобизированный декстран позволяет присоединять мицеллы, липосомы и другие мембранные системы, и так далее.
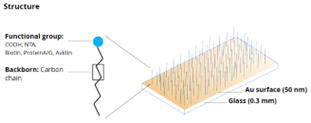
Рисунок 3. Структура поверхности сенсорного чипа
Таким образом, SPR-биосенсор – это достаточно гибкая, универсальная система, которая не требует введения меток и которую можно «настроить» под большое количество практически важных задач. Более того, эта технология является «золотым стандартом» в изучении аффинности и специфичности взаимодействий биомолекул самых разнообразных типов. Поэтому SPR-биосенсоры находят широкое применение в клинической медицине – при диагностике заболеваний, в фармацевтике – при разработке и контроле качества новых лекарств, а также в биомедицине и биоинженерии (см. DOI 10.3390/s150510481).
