В ближайшие несколько лет истекает срок патентной защиты сразу для множества биотехнологических препаратов, которые используются в лечении сложнейших онкологических, эндокринологических и других заболеваний. После окончания патентной защиты на рынке в большом количестве появляются их аналоги. Мы решили немного разобраться, чем такие препараты отличаются от дженериков, что нас ждет через несколько лет и какую роль в этой отрасли сыграет развитие метода кругового дихроизма.
Дженерик и биосимиляр. В чем разница?
Когда у какого-то оригинального препарата заканчивается срок патентной защиты, другие фармкомпании получают право использовать такое же действующее вещество в составе своих препаратов. Такие препараты, воспроизведенные другими производителями, называются термином дженерик (генерик). В российском законодательстве для этой группы препаратов используется определение «воспроизведенное лекарственное средство».
В зарубежной практике, в частности в Евросоюзе и США, считается, что дженерик как препарат, химически идентичный оригинальному, может быть произведен только для химических веществ (на основе малых молекул). А для биотехнологических препаратов произвести из живых организмов полностью идентичный аналог затруднительно. Они представляют собой сложные пептидные молекулы, чаще всего синтезируемые микроорганизмами, с массой от десятков до сотен кД. Белок может быть первичной, вторичной, третичной и четвертичной структуры, которая наиболее подвержена изменениям при незначительных модификациях технологического процесса. В отличие от химических молекул, взаимодействия внутри молекулы белка прогнозировать очень сложно. Таким образом, возможно произвести только похожий препарат — биосимиляр. Встречаются также такие варианты названия как биоаналог, биоаналогичный препарат, биоподобный препарат, follow-on protein products («препарат, подобный белковым лекарственным средствам»).
Особенности разработки и производства биосимиляров
Задача производителей биосимиляров – воспроизвести сложную молекулу и убедиться в том, что копия полностью соответствует оригиналу по структурным характеристикам, физико-химическим свойствам, биологическим активности и так далее.Процедуры одобрения, которые подходят для дженериков, не подходят для биоаналогов. Учитывая сложную пространственную структуру молекул, европейские регулирующие органы разработали руководство для производителей биосимиляров, в котором закрепили необходимость проведения дополнительных клинических исследований биосимиляров, а также установили требование демонстрации иммуногенности воспроизведенного препарата.
В результате тщательного изучения всех расхождений между биосимиляром и оригинальным препаратом производители биосимиляров добиваются такой степени схожести, когда спектроскопические данные обоих препаратов, практически совпадают, отражая не только идентичность состава, но и идентичность структуры.
Процессе изучения образцов молекул ученые могут не просто повторить оригинальную молекулу, но и оставить в ней те изменения, которые кажутся им наиболее полезными.
В некоторых направлениях регуляторы разрешают компаниям проявить свои возможности, и тогда появляются биоаналоги, которые отличаются большим сроком хранения, в том числе вне холодильника, меньшим содержанием примесей, меньшей вариативностью. То есть с биологической точки зрения они идентичны оригинальным, а с потребительской – даже обладают преимуществами.
Перспективы
Биотехнологические лекарственные средства внесли большой вклад в терапию тяжёлых метаболических и дегенеративных заболеваний, таких как сахарный диабет, аутоиммунные заболевания, псориаз, онкологические заболевания и др. Истечение сроков патентной защиты на большинство оригинальных биопрепаратов создало предпосылки к внедрению аналогичных биопрепаратов, так называемых биосимиляров.
Буквально за последние пару лет молекулы биопрепаратов, дающие около половины мировых продаж, уже потеряли патентную защиту. Ожидается, что к 2020 г. продажи биосимиляров превысят 100 млрд $. Среди основных факторов развития рынка биосимиляров называют умеренную цену по сравнению с оригинальными продуктами, широкую сферу применения, увеличение заинтересованности в них государства.
Интересная статья на эту тему, а также будущего биосимиляров в России.
Интересная статья на тему различий между биосимилярами и оригинальными препаратами.
Роль спектроскопии кругового дихроизма в валидации биосимиляров
Итак, мы выяснили, что минимальные изменения в структуре высокого порядка белковой молекулы могут существенно повлиять на эффективность и иммуногенность препарата. И изучение структуры высокого порядка является важной составляющей критических атрибутов качества (CQA, critical quality attribute), которые используются для характеризации структуры, чистоты, функциональных свойств и стабильности потенциальных лекарственных средств.
Спектроскопия кругового дихроизма (КД) позволяет производить сопоставление вторичной и третичной структуры белков, по спектру КД можно определить содержание альфа- и бета-структур в цепочке, оценить упаковку белка. На 5 международном симпозиуме «Symposium on HOS ofProtein Therapeutics 2016» было отмечено, что круговой дихроизм необходим в 96% случаев при работе с биосимилярами на основе моноклональных антител.
Долгое время метод КД являлся сугубо качественным, вследствие несовершенства технологии калибровки. Сопоставление данных производилось на глаз. Однако Applied Photophysics в 2015 году произвели революцию в этой области, представив новый калибровочный стандарт и разработав методику количественного статистического сопоставления структур qCD (quantitative curcular dichroism).
Использование qCD для исследования биопрепаратов
Точность сопоставления структуры высокого порядка должна быть достаточно высокой чтобы обнаружить даже минимальные различия. При такой точности важна воспроизводимость спектральных данных. А это в свою очередь возможно при максимальной автоматизации процесса. Именно поэтому для подобных исследований важно использование автоматизированного КД-спектрометра.
Рассмотрим небольшой пример ниже.
КД-анализ третичной структуры в сильно поглощающем буфере показал различия в области триптофана Fab-фрагментов, ответственных за связывание антитела с антигеном, взятых из разных партий производителя оригинального лекарства.
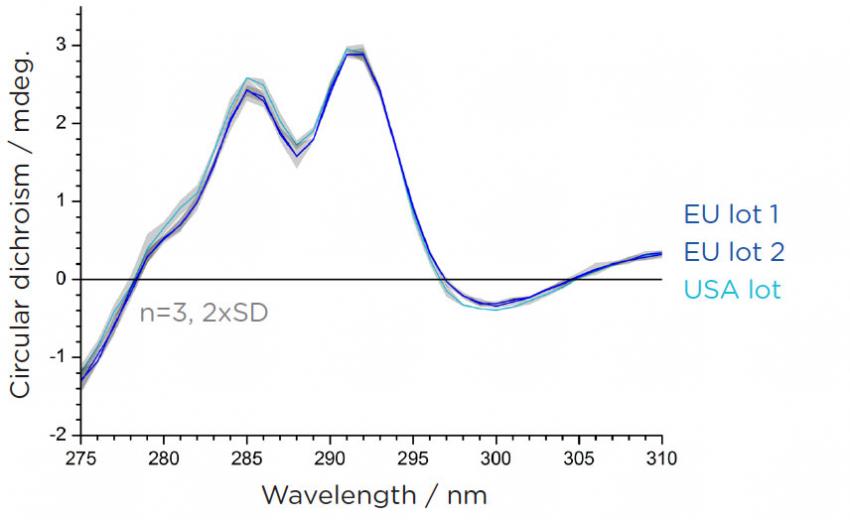
Статистическая обработка полученных данных показала, что разница в структуре образцов препарата из Америки и Европы является значительной, поскольку выходит за пределы двойного стандартного отклонения.
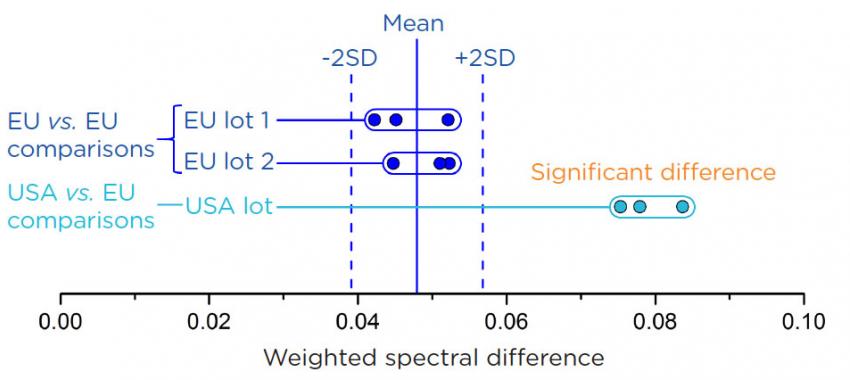
Последующее сравнение биосимиляра с оригинальным лекарством подтвердило значительное статистическое расхождение.
Более детальное рассмотрение примеров выходит за рамки данной статьи. Больше примеров Вы найдете в описании спектрометра Chirascan Q100.
Заключение
Направление биосимиляров является очень перспективным для российских фармацевтических компаний. Лояльное по сравнению с развитыми странами государственное регулирование (а точнее фактическое его отсутствие) открывает путь для упрощенной регистрации этих препаратов по системе дженериков. В то же время с каждым годом все больше оригинальных биотехнологических препаратов теряют патентную защиту, А курс на импортозамещение сохраняется. Так что ожидаем если не бурного, то хотя бы устойчивого развития нашей фарминдустрии в этой области.
